教養学部報
第587号 ![]()
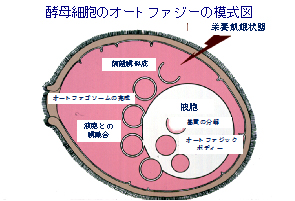
2016年 ノーベル生理学・医学賞の紹介 オートファジーのメカニズムの発見 「かたち」を見ることからはじめる
村田昌之

ノーベル生理学・医学賞のご受賞おめでとうございます!
今年度のノーベル生理学・医学賞に教養学部基礎科学科
(現在は統合自然科学科に改組)、大学院理学系研究科
相関理化学専攻(同専攻の場所は駒場)ご出身の
大隅良典先生(現在東京工業大学栄誉教授)が選出され
ました。 二〇一六年ノーベル生理学・医学賞は、「オートファジーのメカニズムの発見」に大きく貢献した東京工業大学・栄誉教授・大隅良典博士の単独受賞となった。オートファジーとは、「細胞が、飢餓状態などに陥ったとき、自らの細胞質タンパク質やオルガネラなどを消化・分解して、細胞生存に必要なアミノ酸やエネルギー源などとして再利用する仕組み」である。この仕組みは、酵母から高等動植物に至るまで保存されており、単に日常的な細胞内の不良タンパク質やオルガネラなどの処理だけでなく、新生児期の飢餓状態に対する適応、細胞内に侵入した細菌の除去など、細胞の代謝回転を中心に多くの生命活動の場面で利用されている。マスコミでオートファジーを説明するためによく使用されている「リサイクル」という言葉は、ゴミを集めて掃除するだけではなく、そのゴミを材料にした「資源循環」を特徴とするオートファジーの仕組みをうまく表現している。また、その仕組みの破綻は神経変性疾患のよう様々な病態発現に繋がり、その仕組みを抑えることでがんの増殖を抑制することもできるなど、オートファジーのメカニズム研究は、細胞内の重要な分解系の一つとして、また、創薬・医療への戦略指針構築に至るまで、まさに基礎から応用まで大きな研究分野に発展している。
さて、この仕組み(メカニズム)を解明するには、それを駆動する分子情報が必要不可欠であった。しかし、オートファジー過程において、オートファゴソームやオートファジックボディ(AB’s)形成(二面図参照)という形態情報と、それを制御する分子情報を結びつけるのは至難の業である。なぜなら、分子情報抽出の得意な生化学や分子生物学は、細胞の構造(いわゆるタンパク質の働く環境)を壊して、タンパク質やその制御因子を抽出することから始まる。「形態」や「場所」情報は失われる代わりに、現象に関わる分子群のカタログ化と、定量性という科学の重要なパラメーターを得ることができる。一方、オートファゴソーム膜形成のような細胞生物学的研究は、ありのままの「形態」や「場所」の情報を保持しながら、それを制御・駆動する分子情報を得ねばならない。しかし、形態情報は定量化が難しい上に、形態情報から分子情報を抽出する汎用的な手法もほとんど無いのが現状である。それでも、生命の「かたち」(形態)は、その内部で機能する分子群の反応の総体であり、様々な分子情報を内包しているはずである。そこに見える「かたち」から何とか分子情報を引き出したい。この細胞生物学者の果てしない欲求を実現したのが大隅先生といえるのではないだろうか? 通常、タンパク質分解酵素を欠損させた酵母では、飢餓状態にするとオートファゴソーム由来のオートファジックボディーズ(AB’s)が液胞内に分解されずに蓄積する。しかし、オートファジー過程の変異株では、飢餓状態にしても液胞内にAB’sが蓄積しない。大隅先生は、光学顕微鏡をのぞきながら、この「かたち」の異常を指標に変異酵母株を選択し、酵母遺伝学という当時最強の分子同定ツールを使って、形態情報から分子情報(オートファジー過程に必要な遺伝子群)の抽出に成功した。オートファジー過程の酵母変異株を取得することで、各素過程に関わる分子群を同定でき、より詳細なメカニズムを解明できることになった。今から二〇数年前、大隅先生は、岡崎国立共同研究機構(現:自然科学研究機構)の基礎生物学研究所において、酵母研究で同定した分子情報を基にオートファジー研究を動物細胞・個体に展開されていた。私事ではあるが、同じ敷地内の生理学研究所の助教授として、私は「セミインタクト細胞系」という研究ツールを構築して、GFPで可視化した動物細胞オルガネラの細胞周期依存的な形態変化を、蛍光顕微鏡画像から幾つかの素過程に分離し、生化学的手法でその素過程を駆動するタンパク質の研究を始めていた。そして、大隅先生からセミナーに呼ばれ、セミインタクト細胞系は直ぐにでもオートファジー再構成研究に利用すべきという提案を頂いたのが、先生との最初の出会いであった(この再構成の共同研究は、残念ながらまだ実現されていない)。その後、大隅先生は東工大へ招聘され、私は東大駒場に移ったが、「かたち」から分子情報を抽出する科学は今でも様々なカタチとなって続けられている。
 多くの方々は、ノーベル賞受賞後のテレビ番組で、大隅先生が真剣に顕微鏡をのぞき込む姿や酵母の電子顕微鏡写真の前に立って楽しそうに説明なさっている姿を何度も目にされたことだろう。大隅先生のオートファジー研究はまさしく顕微鏡下の酵母の中で動く膜構造体を観察し、その「かたち」ができる仕組みに思いを馳せることから始まったのである。そして、その研究の「はじまり」は東大・教養学部・三号館のそう広くない研究室だった。そこで動き出した、「かたち」への思いが、「そっと」そして「熱く」ノーベル賞に向かい始めたのだと思う。
多くの方々は、ノーベル賞受賞後のテレビ番組で、大隅先生が真剣に顕微鏡をのぞき込む姿や酵母の電子顕微鏡写真の前に立って楽しそうに説明なさっている姿を何度も目にされたことだろう。大隅先生のオートファジー研究はまさしく顕微鏡下の酵母の中で動く膜構造体を観察し、その「かたち」ができる仕組みに思いを馳せることから始まったのである。そして、その研究の「はじまり」は東大・教養学部・三号館のそう広くない研究室だった。そこで動き出した、「かたち」への思いが、「そっと」そして「熱く」ノーベル賞に向かい始めたのだと思う。
今では、世界中の研究者が医薬応用へと展開させているオートファジー研究であるが、肝心のオートファゴソーム形成の基となり、細胞質に突然出現する隔離膜の発生メカニズムの詳細は不明である。このオートファジー過程の「はじまり」の仕組み解明は、今でも大隅先生の生涯をかけた研究テーマとなっている。大隅先生が、約三〇年前、ここ駒場キャンパスの教養学部で、なぜ「人がやらない研究」をはじめられたのか? その答えは、この隔離膜の発生のように偶発的に見えるが何か必然的な理由がありそうに思った。受賞後のお忙しいスケジュールの間をぬってそのことを伺ってみた。「駒場へ着任したときは一人だったので、何でも自由な考えでテーマを選び、自由にはじめられたからかな?」というお答えが返ってきた。何か人のやらないことをはじめるのには、隔離膜の発生と同じように、ある意味で飢餓感があるときにこそ「はじめられる」ことがあるのだと愉快に思った。
(生命環境科学/化学)
無断での転載、転用、複写を禁じます。

